LA NATURALEZA DEL ENLACE QUÍMICO
Un enlace químico es la fuerza de atracción que mantiene unidos a los átomos en las distintas agrupaciones atómicas. Los átomos se juntan para formar moléculas y compuestos más estables. Se distinguen tres tipos de enlace: covalente, iónico y metálico.
ENLACE COVALENTE
Un enlace covalente entre dos átomos o grupos de átomos se produce cuando estos, para alcanzar el octeto estable, comparten electrones del último nivel. La diferencia de electronegatividades entre los átomos no es suficiente.
De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se suelen producir entre elementos gaseosos o no metales.
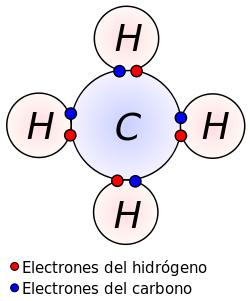
El enlace covalente se presenta cuando dos átomos comparten electrones para estabilizar la unión.
A diferencia de lo que pasa en un enlace iónico, en donde se produce la transferencia de electrones de un átomo a otro; en el enlace covalente, los electrones de enlace son compartidos por ambos átomos. En el enlace covalente, los dos átomos no metálicos comparten uno o más electrones, es decir se unen a través de sus electrones en el último orbital, el cual depende del número atómico en cuestión. Entre los dos átomos pueden compartirse uno, dos o tres pares de electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple respectivamente. En la representación de Lewis, estos enlaces pueden representarse por una pequeña línea entre los átomos.
EL ENLACE IÓNICO
En Química, un enlace iónico o electrovalente es la unión de átomos que resulta de la presencia de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto químico simple.

EL ENLACE METÁLICO
Los átomos de los metales poseen pocos electrones en su capa más externa. El enlace metálico se forma cuando las capas electrónicas exteriores de los átomos metálicos se solapan y se crea un mar de electrones deslocalizados. Los metales son buenos conductores térmicos y de la electricidad, tienen elevados puntos de fusión y ebullición y son dúctiles y maleables.

CANTIDAD DE SUSTANCIA. MOL Y MASA MOLAR
Un mol es la cantidad de sustancia de un sistema que contiene tantas entidades elementales como átomos hay en 0,012 kg (12g) de carbono-12. La masa molar es la masa de un mol de átomos, moléculas, iones, etc.
No hay comentarios:
Publicar un comentario